Proteintech中国公司品牌商
18 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
推荐产品
公司新闻/正文
Cell Res | 细胞焦亡新进展!厦门大学吴乔团队发现甘露糖抑制GSDME介导细胞焦亡的新机制,可有效降低化疗的毒副作用!
5057 人阅读发布时间:2023-09-08 17:06
细胞焦亡(pyroptosis)是一种由 gasdermin(GSDM)蛋白家族成员执行的、受调节的细胞死亡,在拮抗感染和内源性危险信号以及肿瘤等疾病治疗方面发挥重要作用。
此前,在厦门大学吴乔教授团队的研究中,他们发现铁剂可作为增敏剂来促进临床药物诱导 GSDME 介导细胞焦亡的发生。由于黑色素瘤细胞特异性高水平表达 GSDME,且抵抗细胞凋亡,因此铁剂可能是黑色素瘤治疗的潜在方案。
但是,GSDME 在正常细胞中也能够中高水平表达,不适当的焦亡激活会导致正常组织损伤。邵峰院士团队和其他课题组也曾证实,GSDME 介导的焦亡与诱导化疗不良反应相关。因此,对于接受化疗的患者而言,迫切需要能够控制焦亡诱导组织损伤的联合治疗方案。
近日,吴乔教授团队取得突破,在知名期刊《Cell Research》(IF = 44.1)上发表了题为「Mannose antagonizes GSDME-mediated pyroptosis through AMPK activated by metabolite GlcNAc-6P」最.新成果,该研究弥补了上述空缺。

原文链接:https://www.nature.com/articles/s41422-023-00848-6
该文章展示了甘露糖对 GSDME 介导焦亡的抑制作用。在这一过程中,甘露糖通过提升代谢物 GlcNAc-6P 水平以激活 AMPK,激活后的 AMPK 磷酸化 GSDME 从而阻断 caspase-3 的结合和切割,由此抑制细胞焦亡。
在此基础上,研究团队还把甘露糖引入临床化疗过程,发现甘露糖可以作为辅助药物减轻化疗引起的不良反应。
研究结果
1. 甘露糖逆转 GSDME 介导的焦亡
首先经过筛选,研究团队发现无论是铁剂+羰基氰hua物间氯.苯腙(CCCP)还是 raptinal(caspase-3 激活剂)诱导的细胞焦亡,甘露糖均可有效逆转,而其他己糖(葡萄糖、果糖、半乳糖和岩藻糖)则不具有这种作用。这表明甘露糖可能是针对 GSDME 依赖性焦亡的抑制剂。
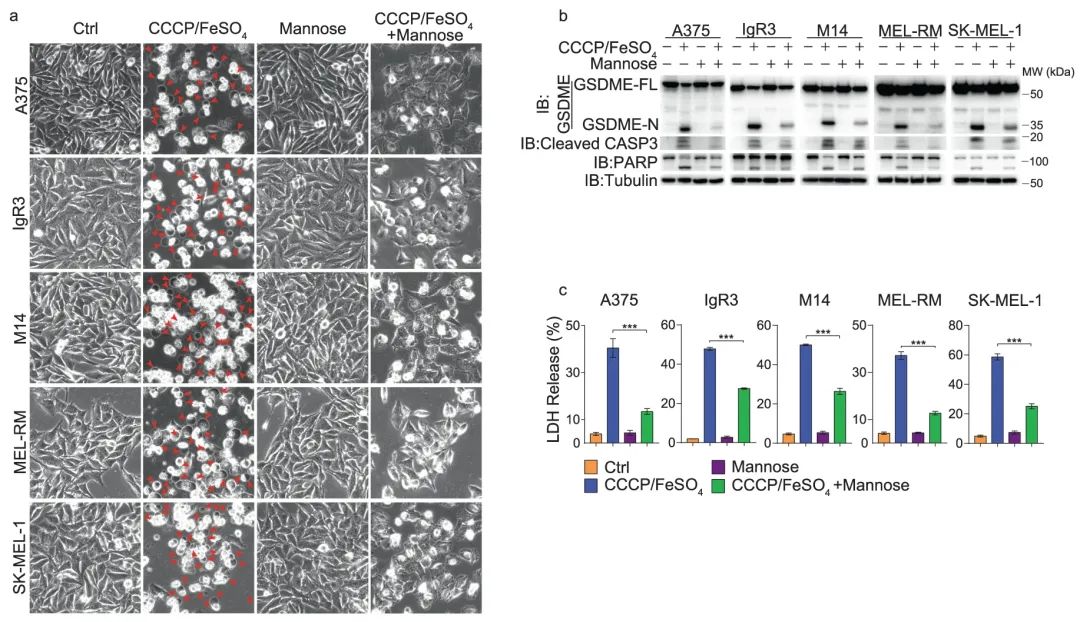
图 1 甘露糖逆转 GSDME 介导的焦亡
2. 氨基己糖生物合成途径(HBP)有助于甘露糖逆转焦亡
那么,甘露糖抑制焦亡通过哪种代谢途径?
通过敲除甘露糖代谢三条途径中关键酶,团队发现,双重敲除己糖胺生物合成途径(HBP)中谷氨酰胺果糖-6-磷酸转氨酶 1/2(GFAT1/2)和第一限速酶,或单独敲除葡萄糖 6-N-乙酰基转移酶 1(GNPNAT1)后,甘露糖对焦亡的抑制作用被消除。这表明甘露糖代谢流向 HBP 可能是甘露糖对焦亡抑制作用的先决条件。
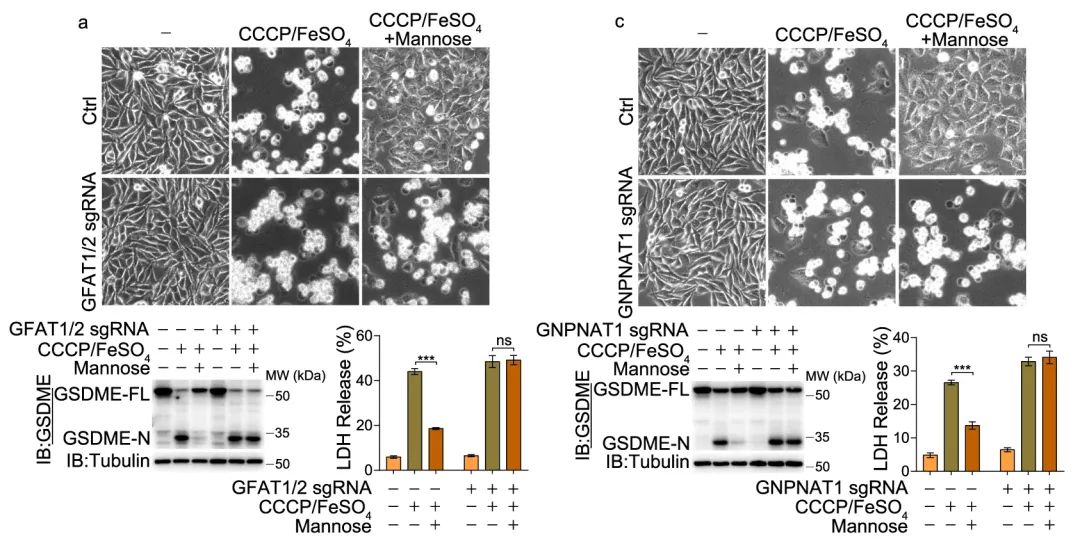
图 2 HBP 中关键酶(GFAT1/2、GNPNAT1)的缺失损害了甘露糖对焦亡的抑制作用
3. 甘露糖诱导 AMPK 磷酸化减轻焦亡
此前有报道显示,甘露糖与骨内瘤细胞中 AMPK 激活相关。该研究也发现类似结果,在 A375 细胞中,甘露糖单独或与 CCCP+铁剂一起大大增加了 Thr172 处的 AMPK 磷酸化。
为了测试 AMPK 激活是否与焦亡抑制相关,团队使用不同浓度的甘露糖处理细胞。随着甘露糖浓度的增加,AMPK 磷酸化逐渐增加,从而导致焦亡被抑制。在抑制/敲除 AMPK 后,这种情况消失。因此,甘露糖通过激活 AMPK 来抑制焦亡。
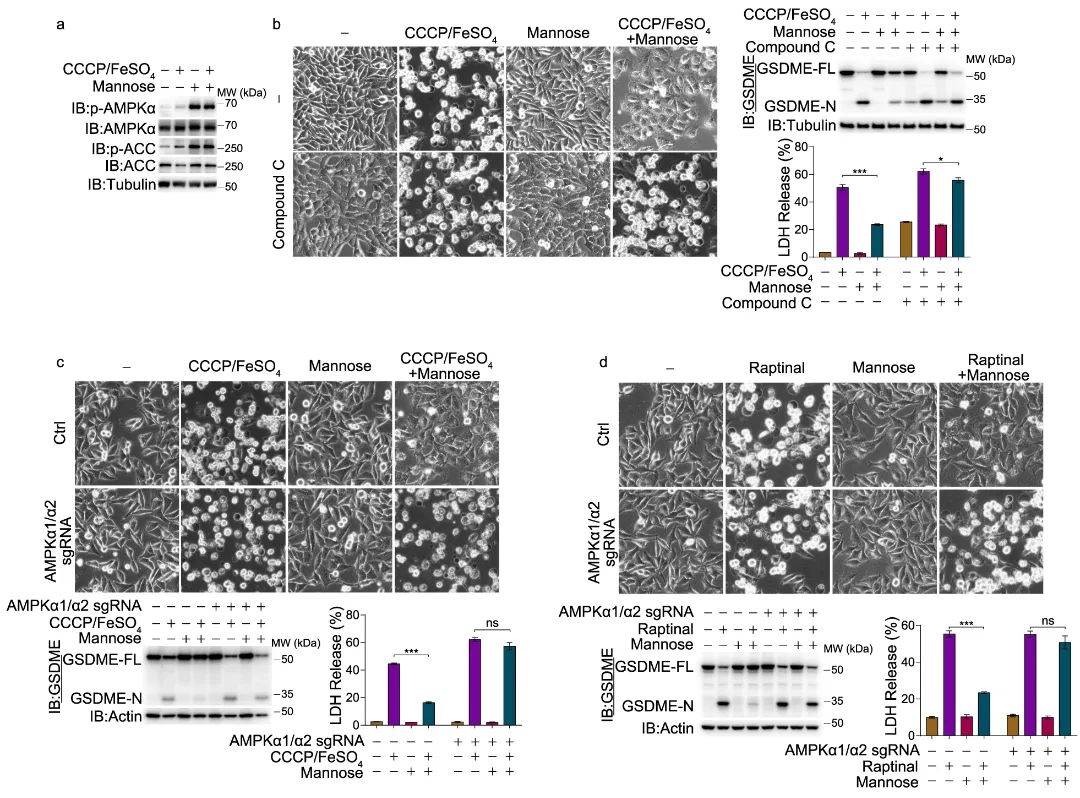
图 3 AMPK 的抑制导致甘露糖对焦亡的抑制失效
4. HBP 中的代谢物 GlcNAc-6P 靶向并激活 AMPK
团队进一步探讨了甘露糖诱导 AMPK 激活的机制。由于甘露糖不影响 HBP 通路中酶的水平,团队假设 HBP 中的代谢物可能激活 AMPK。结果印证了这一猜想,HBP 代谢物 GlcNAc-6P(与 AMPKα 结合促进后者与激酶 LKB1 相互作用从而磷酸化)和 GlcNAc-1P(轻微作用)对 AMPK 活性存在影响。

图 4 GlcNAc-6P 直接结合并激活 AMPKα
(d:敲除 LKB1 抑制了 GlcNAc-6P 或甘露糖对 AMPKα 磷酸化的影响;e:GlcNAc-6P 直接结合 his-AMPKα1;f:GlcNAc-6P 或甘露糖作用下 AMPKα1 与 LKB1 的相互作用显著增加;h-i:甘露糖诱导的 AMPKα1-LKB1 相互作用的增强依赖于 HBP)
5. AMPK 磷酸化 GSDME 以阻断 caspase-3-介导的切割
那么,AMPK 被激活如何对 GSDME 产生影响?
团队发现,AMPK 不与 caspase-3 作用,而是与 GSDME 直接相互作用。质谱结果进一步确定,AMPK 可诱导 GSDME 在 Thr6 位点强磷酸化。同时,这种磷酸化直接影响 caspase-3 对 GSDME 的识别。这都说明,甘露糖激活的 AMPK 可能通过在 Thr6 处磷酸化 GSDME 来诱导 GSDME 的构象变化,从而干扰 GSDME 和 caspase-3 之间的相互作用。

图 5 磷酸化突变体 GSDMET6E 对 caspase-3 介导的体外切割具有抗性且其结构不同于野生型 GSDME
6. 甘露糖抑制顺铂诱导的正常细胞系和类器官的焦亡
上面提到,GSDME 通常会在正常细胞高表达,在很多癌细胞中低表达。并且据报道,GSDME 介导的正常组织焦亡是化疗诱导损伤的主要原因。因此团队测试了甘露糖对正常细胞和类器官是否具有保护作用。
结果显示,正常细胞中顺铂也会诱导焦亡,并且这一过程同样会被甘露糖抑制;在构建的小肠类器官中,也是类似的结果,并且随着 GSDME 的敲除,顺铂药物对类器官的毒害作用也随之消失了。
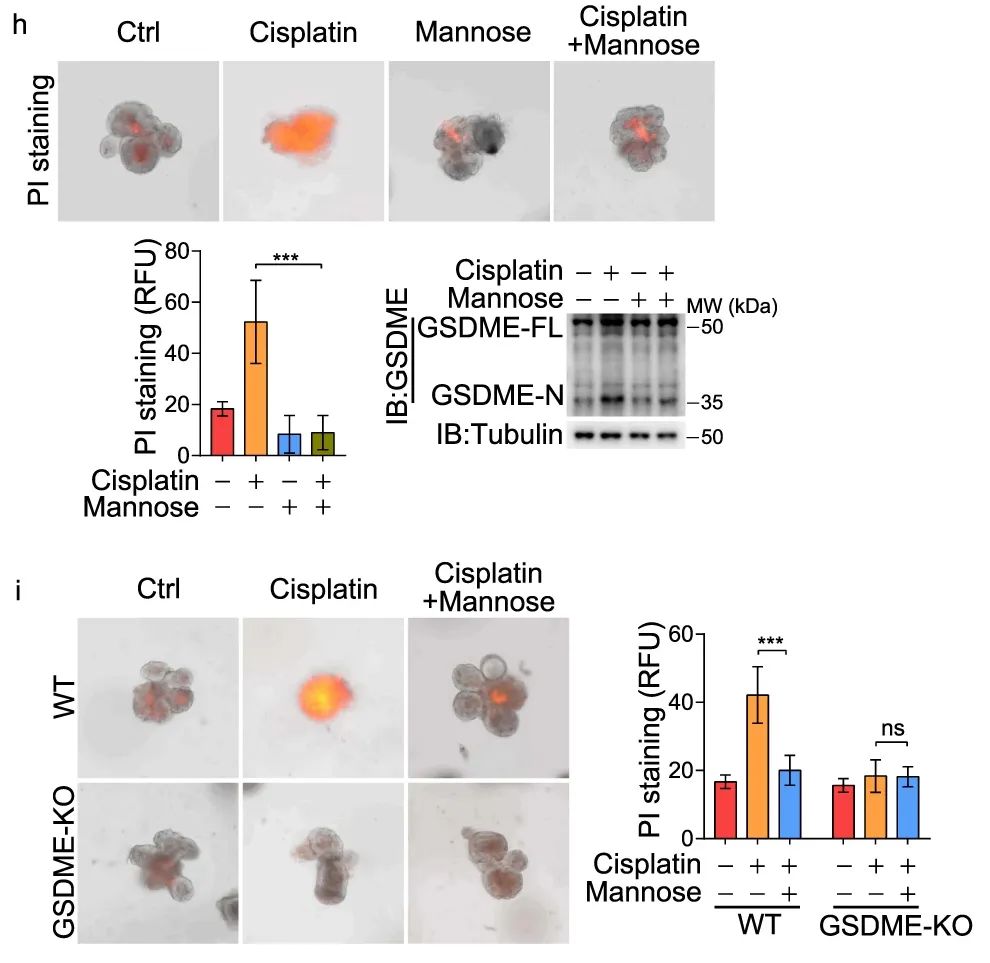
图 6 甘露糖抑制顺铂诱导的类器官细胞焦亡
7. 甘露糖在小鼠模型中保护正常器官免受化疗诱导损伤
在此基础上,团队测试了甘露糖在体内的保护作用。在小鼠模型肠和肾等不同组织中均观察到:甘露糖能够避免这些体内组织受到顺铂诱导的毒性影响。这些变化也伴随着甘糖露存在下 AMPK 磷酸化的增加和 GSDME 切割的减少。同时团队还验证了这种保护作用也通过 AMPK 诱导的 GSDME Thr6 磷酸化执行。
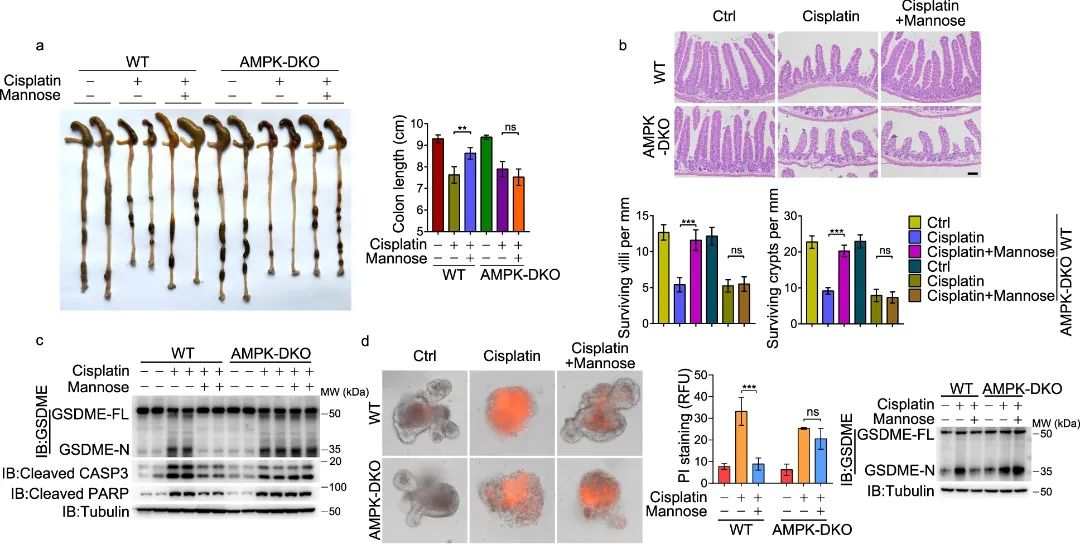
图 6:甘露糖保护正常器官免受化疗药物诱导损伤
8. 甘露糖与化疗药物联合治疗小鼠和临床患者的原发性肿瘤
为了验证甘露糖和化疗药物联合使用能否达到肿瘤治疗的效果,团队建立了小鼠原发性肝癌模型。顺铂给药明显延缓肝癌进展(促进肝癌细胞发生凋亡),但也诱导肠道和肾脏的急性损伤(诱导正常细胞发生焦亡)。
甘露糖联合治疗不影响顺铂对肿瘤组织的作用,但能有效改善顺铂诱导的肠和肾损伤(抑制正常细胞的焦亡)。另一种化疗药物奥沙利铂联用甘露糖也出现相同的保护作用。此外,甘露糖对小鼠血糖水平没有明显影响。这说明化疗+甘露糖的方式可能是临床癌症治疗的可行策略。
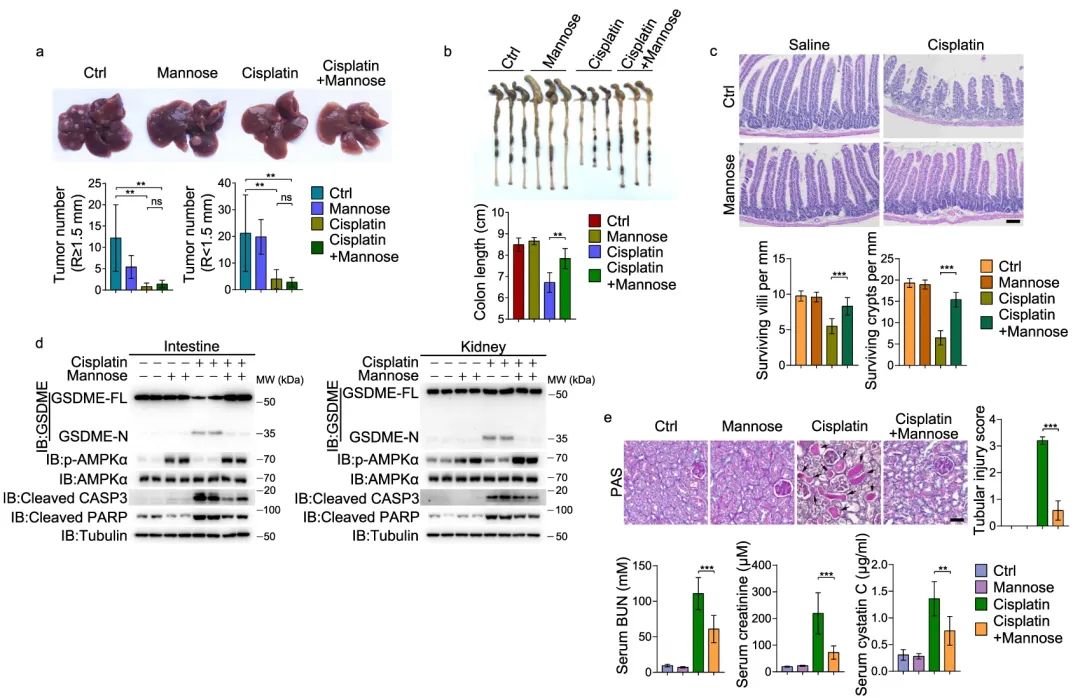
图 7 甘露糖拯救顺铂化疗诱导的肠、肾损伤
最后,为了评价甘露糖减轻化疗副作用的有效性,团队招募了 8 名接受 XELOX 化疗方案的胃肠癌患者。XELOX 化疗联用甘露糖方案可明显降低胃肠道癌症患者排便频率和粪便中白细胞数量,同时其血清生化指标水平更趋于正常。这些临床数据充分证明了甘露糖作为临床化疗辅助药物缓解患者不良反应的前景。
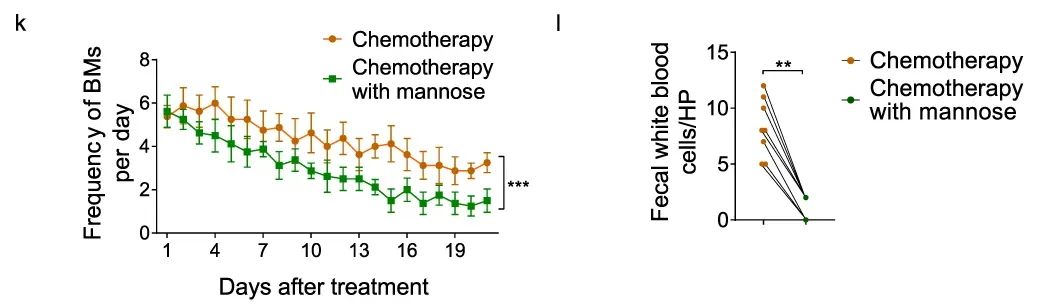
图 8 XELOX 化疗联用甘露糖方案缓解患者不良反应
研究结果
总而言之,吴乔教授团队揭示了一条甘露糖负调控细胞焦亡的全新途径:
甘露糖进入细胞后,通过己糖胺生物合成途径(HBP)提高代谢物 N-乙酰氨基葡萄糖-6-磷酸(GlcNAc-6P)的含量,GlcNAc-6P 结合并激活 AMPK,活化的 AMPK 进一步磷酸化 GSDME,进而阻碍 caspase-3 对 GSDME 的识别和切割,最终抑制细胞焦亡的发生。

图 9 甘露糖作用机制示意图
更令人惊喜的是,在小鼠模型和临床患者中,团队发现甘露糖联合化疗药物治疗不仅不影响化疗药物对肿瘤组织的杀伤作用,还能够保护正常器官免受化疗药物诱导的损伤;而且甘露糖本身是一种天然产物,被广泛用于食品添加和临床疾病治疗,其安全性具有保障。因此甘露糖很有潜力成为一种避免化疗毒副作用的联合治疗方案。
抗体推荐
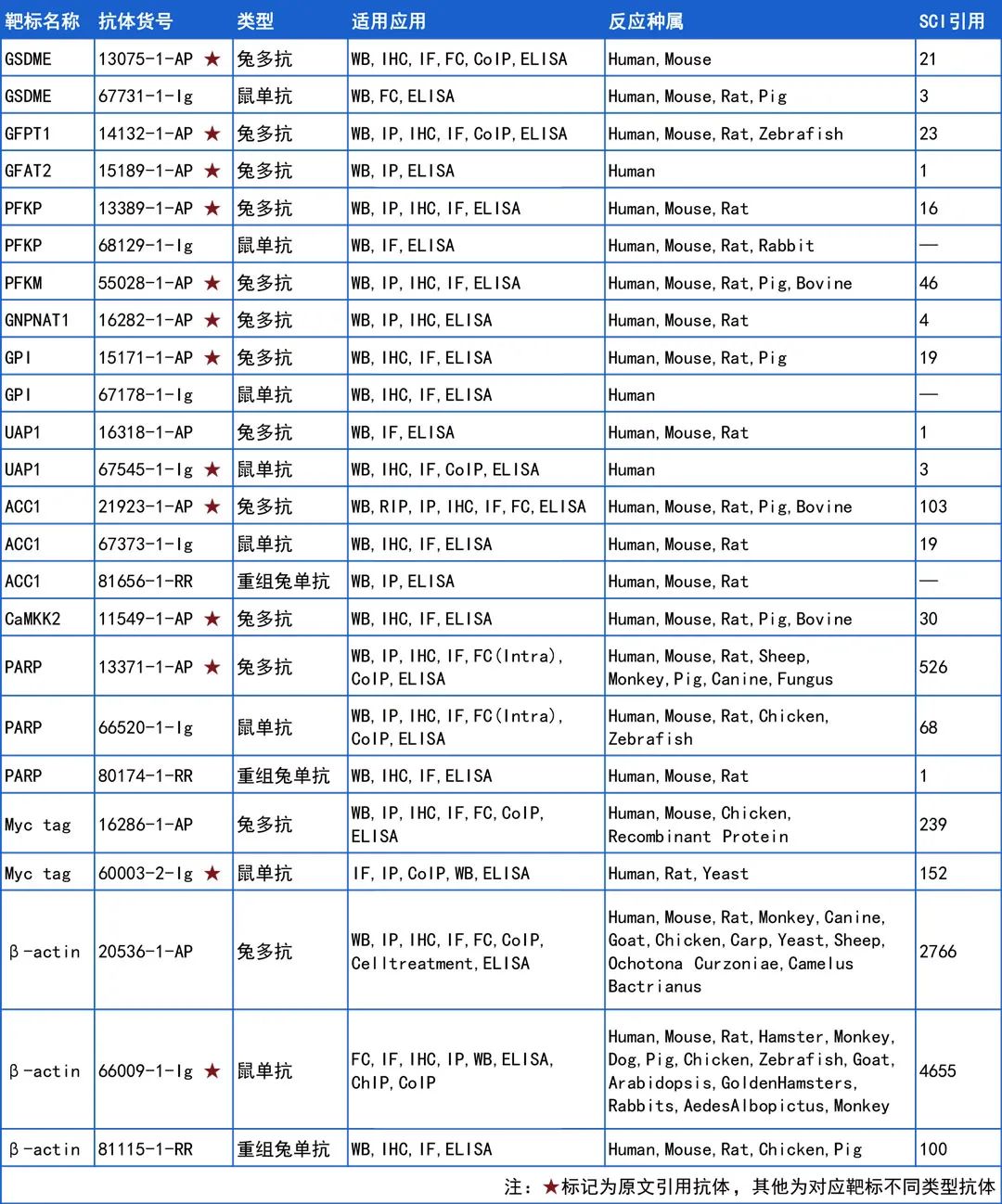
值得一提的是,在上述研究中 GSDME、GFAT1/GFPT1 、GFAT2、PFKP、PFKM、GNPNAT1、GPI、UAP1、ACC1、CaMKK2 和 PARP 等 13 个关键靶标抗体来源于 Proteintech!感谢团队的信任!这里小 P 将文章引用抗体信息汇总,希望对相关领域的研究带来帮助!
更多细胞焦亡研究相关产品,可直接咨询下方客服;
如需订购,请联系当地授权代理商 ~
最后祝大家实验顺利,成果多多!






